
Ինչպես արդեն գիտեք, ատոմը կազմված է միջուկից և էլեկտրոնային թաղանթից: Ատոմն էլեկտրաչեզոք է, քանի որ էլեկտրոնների գումարային լիցքը համակշռում է միջուկի դրական լիցքը:

Այն քիմիական տարրերը, որոնք ունեն նույն կարգաթիվը, այսինքն նույն թվով պրոտոններ, սակայն տարբեր ատոմային զանգվածներ, կոչվում են իզոտոպներ:
Միևնույն քիմիական տարրի իզոտոպները միմյանցից տարբերվում են նեյտրոնների թվով:
Օրինակ՝ ջրածնի 11H իզոտոպներն են դեյտերիումը՝ 12 H և տրիտիումը՝ 3 1H
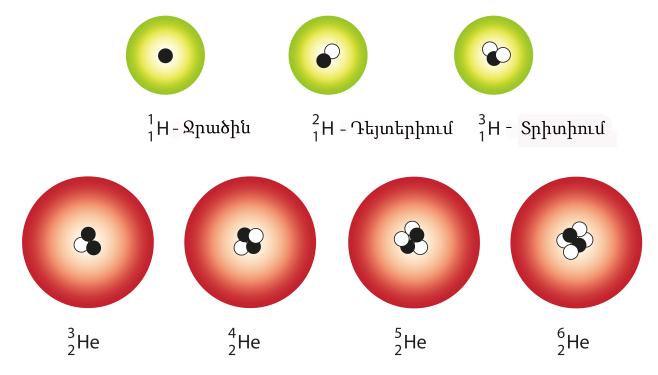
Ջրածնի միջուկը կազմված է 1 պրոտոնից, դեյտերիումինը՝ 1 պրոտոնից և 1 նեյտրոնից:
Տրետիումի միջուկը կազմում են 1 պրոտոն և 2 նեյտրոնը:
Հայտնի նաև He-ի 4 իզոտոպներ՝32He,42He,25He,62He
Պրոտոնների թվով պայմանավորված է ատոմի քիմիական հատկությունները, իսկ նեյտրոնների թվով՝ տվյալ քիմիական տարրի ատոմային զանգվածը:
